乳腺癌的发病率和死亡率日益升高,已成为威胁人类生命健康的主要癌症类型之一。癌症的靶向治疗具备精准、可控、毒副作用小等优势,其快速发展可为乳腺癌患者提供了更好的治疗选择。由于乳腺癌的致病机制复杂,当前可用的小分子靶向药物仍然非常有限。
哺乳动物雷帕霉素靶蛋白(mTOR)是PI3K-Akt-mTOR信号通路下游关键调控蛋白,在细胞生长、增殖、迁移、代谢、凋亡及自噬等生理过程中发挥重要作用,其异常激活与癌症的发生与发展密切相关,特别是乳腺癌。靶向mTOR激酶是近年来小分子抗肿瘤药物研究的热点,尽管取得了一些进展,但迄今尚无小分子抑制剂上市。由于PI3K相关激酶家族蛋白序列高度同源,使得开发选择性mTOR激酶抑制剂面临较大挑战;同时低选择性抑制带来的非靶点相关副作用也引起研究人员极大的关注。
近日,威斯尼斯化学药工程中心汤磊/张吉泉团队在国际知名期刊《Journal of Medicinal Chemistry》(IF: 7.3,药物化学TOP1)上在线发表研究论文“Design, Synthesis, Formulation, and Bioevaluation of Trisubstituted Triazines as Highly Selective mTOR Inhibitors for the Treatment of Human Breast Cancer”。该研究采用基于结构的药物分子设计策略,以三期临床候选药物Gedatolisib(PT-1)为工具分子,通过结构改造筛选出高选择性mTOR抑制剂PT-88,该化合物具有较强的抗乳腺癌活性,有良好的临床开发前景。

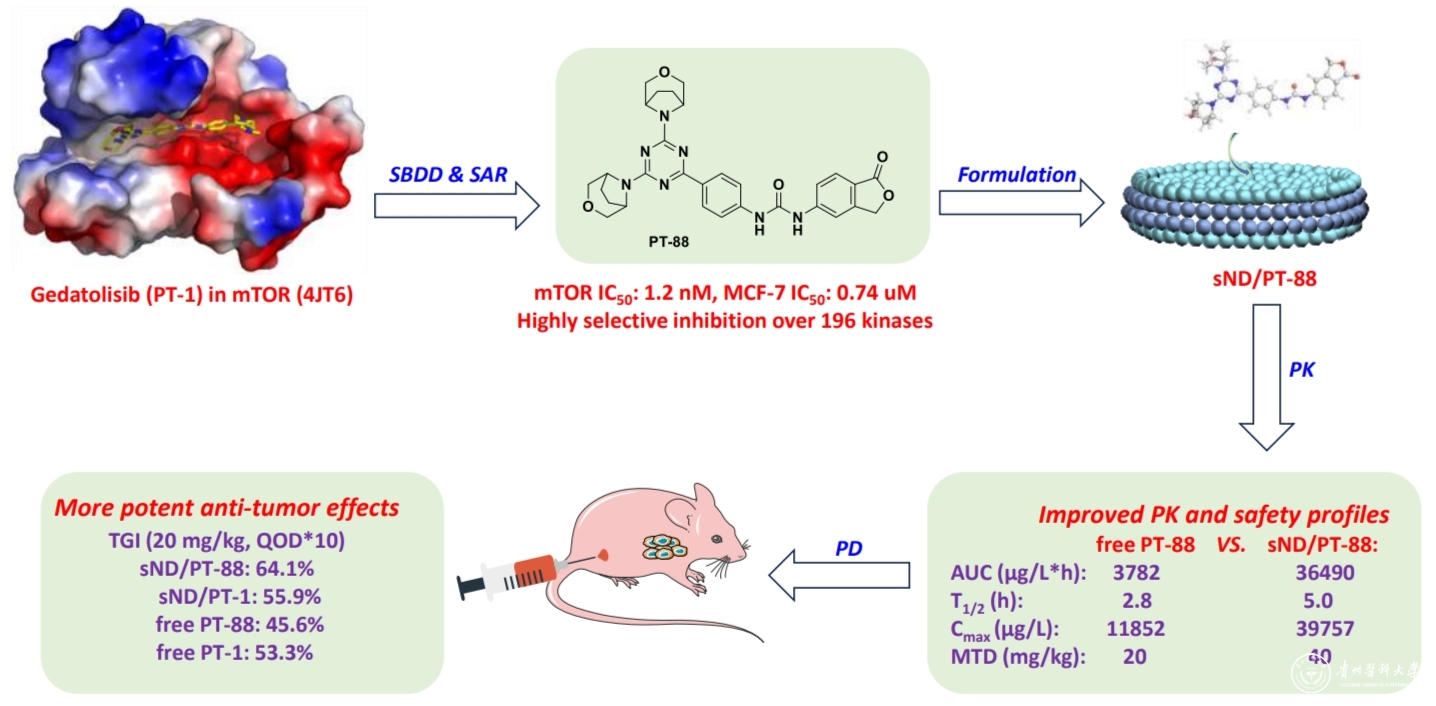
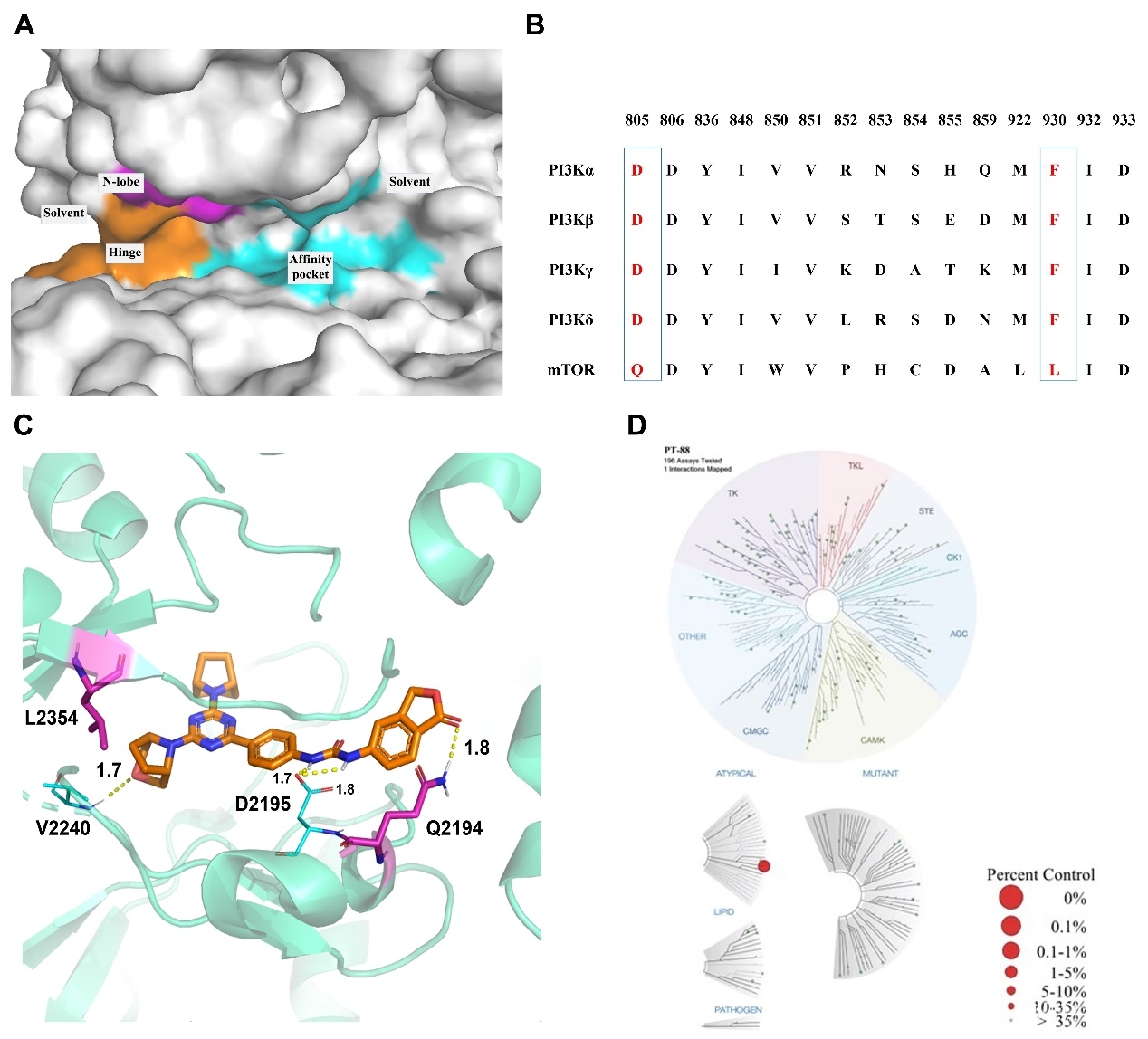
汤磊/张吉泉团队近年的主要研究方向之一是围绕恶性肿瘤及其发病机制,基于PI3K-Akt-mTOR信号通路开展创新药物研究,取得了系列创新性成果(J. Med. Chem.,2016, 59, 7268-7274;Eur. J. Med. Chem.,2020, 204, 112637;Eur. J. Med. Chem.,2022,229, 114055;Bioorg. Chem.,2023, 140, 106781;Eur. J. Med. Chem.,2023,260 115754.)。近期,该团队以泛PI3K/mTOR抑制剂PT-1作为工具分子,根据PI3Ks及mTOR蛋白序列上关键残基的不同,开展理性药物分子设计,经过两轮构效关系研究最终发现了高活性mTOR抑制剂PT-88(IC50:1.2 nM)。激酶谱测试显示(196种激酶),PT-88专一性地结合mTOR,显示出极高的选择性。研究进一步通过分子动力学(MD)、关键残基自由能分解及丙氨酸扫描突变等技术对PT-88的分子结合模式进行了分析。
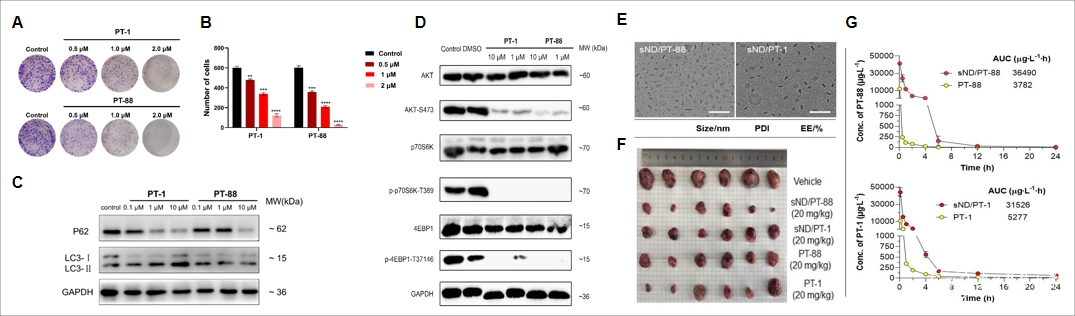
化合物PT-88对乳腺癌细胞株MCF-7具有较好的选择性和抗增殖活性(0.74μM),通过细胞克隆形成、划痕、周期阻滞、凋亡、自噬及信号通路抑制等实验考察了化合物的抗肿瘤机制。为改善优选化合物的药动学性质,课题组与复旦大学占昌友教授课题组合作,制备了PT-88及阳性对照PT-1的脂质纳米圆盘制剂(sND/PT-88和sND/PT-1)。结果显示,成制剂后PT-88的血浆暴露量提高了近10倍,半衰期及最大血药浓度均显著改善。值得注意的是,制剂同时极大地提升了化合物的体内耐受剂量(MTD)。BALB/c裸鼠药效学研究显示,20 mg/kg剂量给药后(i.v., QOD´10),sND/PT-88给药组的肿瘤生长抑制率(TGI)达到64.1%,显著优于sND/PT-1(55.9%)及游离药物PT-88组(45.6%),且具有较好的体内安全性。
该研究通过基于结构的药物分子设计策略,成功筛选出高活性与选择性mTOR抑制剂PT-88,化合物已获发明专利授权保护(ZL202210435526.7)。研究为基于mTOR激酶的创新药物研究提供了新的工具分子,也为候选药物分子进入临床评价提供了新的研究范式。
本研究由汤磊/张吉泉教授团队、复旦大学占昌友教授团队以及华南理工大学王领教授团队共同完成。硕士生孙琪雯为论文第一作者,王领、汤磊、占昌友、张吉泉为论文共同通讯作者。该研究得到了国家自然科学基金(82060625, 22267003)、贵州省自然科学基金(ZK[2023]305),贵州省优秀青年科技人才计划(YQK[2023]030)、澳门威斯尼斯WNS888入口优秀青年人才计划([2022]102)及澳门威斯尼斯WNS888入口柔性人才计划(RN21047)等基金资助。
原文链接:https://pubs.acs.org/doi/10.1021/acs.jmedchem.4c00173
 公网安备
公网安备