近日,药学院沈祥春教授与附属医院李海洋教授团队在天然倍半萜类小分子药物改善类风湿性关节炎研究方面取得新进展,相关研究以“Small molecule α-methylene-γ-butyrolactone, an evolutionarily conserved moiety in sesquiterpene lactones, ameliorates arthritic phenotype via interference DNA binding activity of NF-κB”为题发表于国际权威刊物《Acta Pharmaceutica Sinica B》(中科院1区药学TOP期刊,2023年最新IF=14.5)。

类风湿性关节炎(Rheumatoid arthritis, RA)是一种复杂的自身免疫病,其常伴随异常的炎症性滑膜增生以及软骨和骨骼的损伤,严重影响患者的健康和生活质量。目前采用的常规药物未能完全治愈RA或具有一定不良反应。因此,寻找潜在的RA治疗靶点和治疗药物至关重要。
倍半萜内酯(Sesquiterpene lactones, SLs)是一类源于菊科植物的活性小分子化合物,它们在多种炎症模型中表现出较强的抗炎活性。然而,获取方式繁琐、含量不高等原因限制了其应用。大量研究提示,α,β-不饱和酮结构广泛存在于抗炎SLs中,一些具有该结构的SLs在抗炎和RA治疗方面显示出巨大的潜力。
从前期研究中发现的一些实验现象和文献报道中受到启发,研究者系统总结了具有抗炎活性的SLs的主要骨架类型(包括吉马内酯,愈创木内酯,伪愈创木内酯,桉烷内酯和heliangolides等)并从中获得以下启发:大部分的抗炎SLs都包含一个α-亚甲基-γ-丁内酯(α-methylene-γ-butyrolactone,α-M-γ-B)核心结构,这表明α-M-γ-B可能在抗炎SLs中具有关键作用。受此启发,研究者获取了SLs结构简化的小分子α-M-γ-B和其他六种结构类似物。相较于其他几个类似物,α-M-γ-B表现出最强的亲电性和最强的体外抗炎活性。α-M-γ-B相较于常见的抗炎药物(阿司匹林、地塞米松等)具有更强的体外抗炎活性。研究者进一步证实α-M-γ-B通过调控巨噬细胞的极化状态改善滑膜微环境缓解小鼠关节炎表型。此外,研究者发现α-M-γ-B虽然不抑制核转录因子NF-κB的入核,但是α-M-γ-B可以直接靶向NF-κB p65上的半胱氨酸残基并干扰其与DNA的结合,进而发挥抗炎和RA治疗作用。
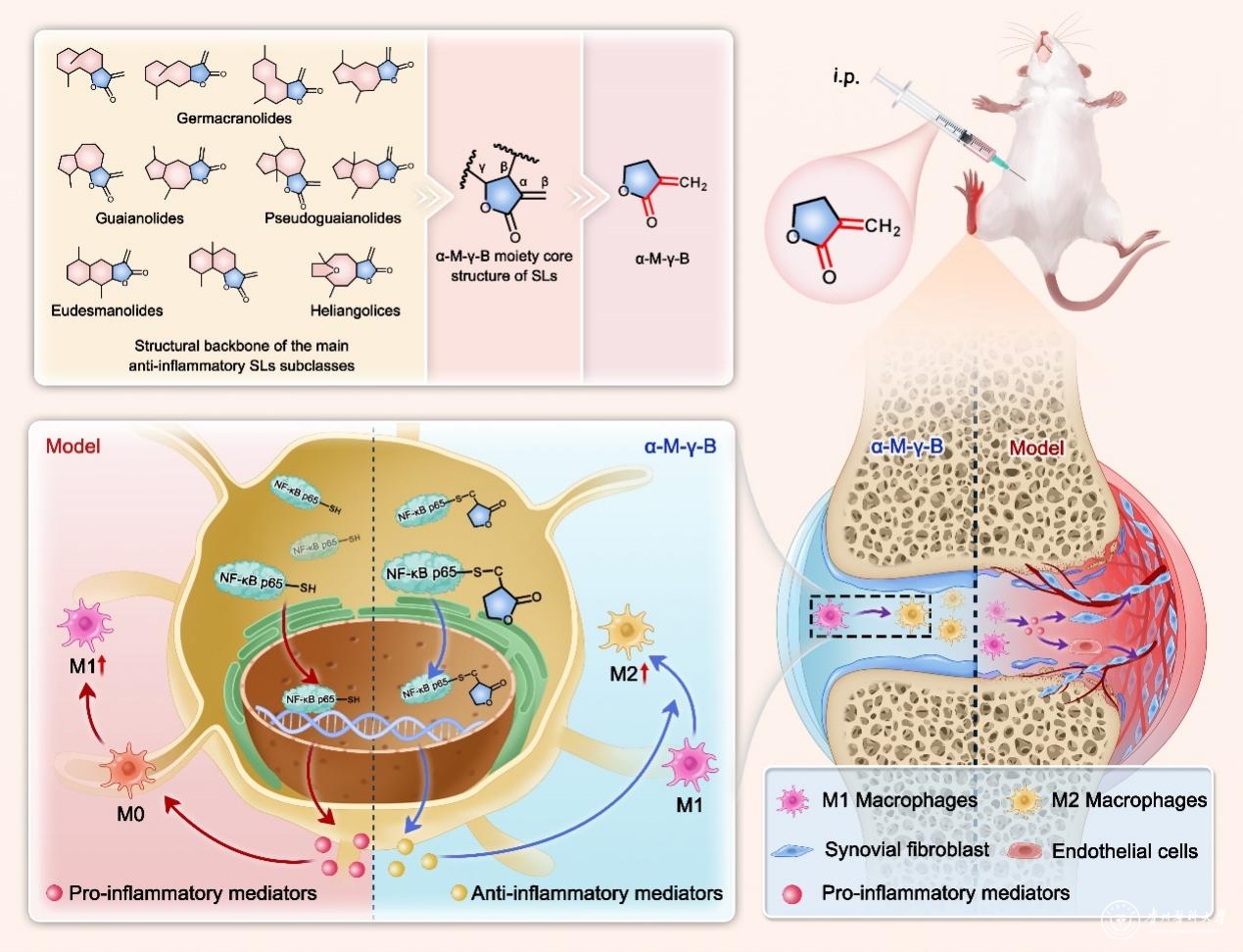
综上所述,本研究揭示了α-M-γ-B结构在抗炎SLs中高度进化保守这一特征,基于这一结构特征获得的结构简化小分子α-M-γ-B表现出较好的抗炎和RA治疗潜力,为SLs类天然小分子在炎症性疾病治疗药物中的开发提供了宝贵的信息参考。
本研究由沈祥春教授团队和附属医院李海洋教授团队合作完成,澳门大学中华医药研究院余华教授对于本研究的开展给予了大力支持。药学院副教授令狐克刚博士后为本论文的第一作者,崔文清和李太琴两位研究生为本论文的共同第一作者。胡晓霞、李海洋、沈祥春为本论文共同通讯作者。该研究是在国家自然科学基金项目(82260801)、中央引导地方基金([2023]003)、贵州省高层次创新人才十层次项目(GCC[2023]048)、中国博士后科学基金面上项目(M730815)、澳门威斯尼斯WNS888入口青年拔尖人才项目(2023110)等项目支持下完成。
文章链接:https://www.sciencedirect.com/science/article/pii/S2211383524001321
 公网安备
公网安备